CakapCakap – Cakap People! Merck & Co mengatakan pada hari Jumat, 26 November 2021, data terbaru dari studinya terhadap pil eksperimental COVID-19 menunjukkan obat itu secara signifikan kurang efektif dalam mengurangi rawat inap dan kematian daripada yang dilaporkan sebelumnya.
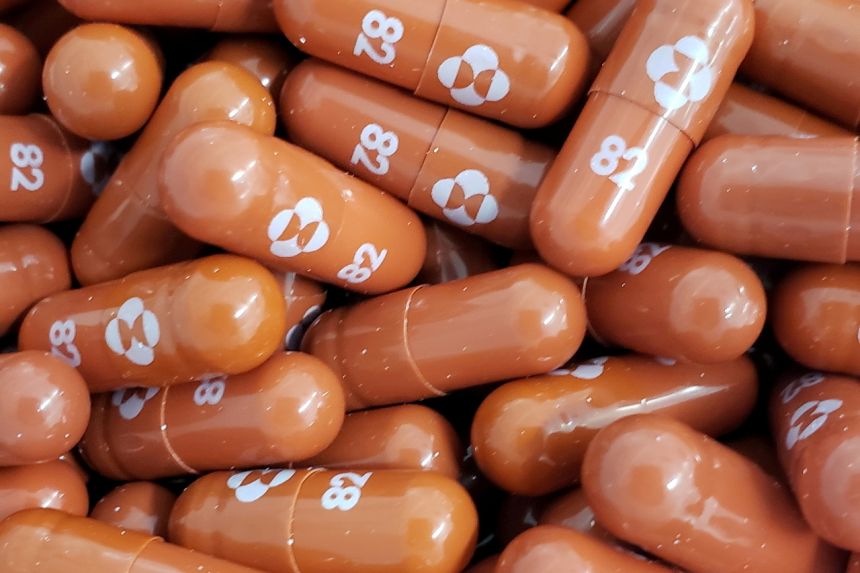
Reuters melaporkan, produsen obat itu mengatakan pilnya menunjukkan pengurangan 30% dalam rawat inap dan kematian, berdasarkan data dari 1.433 pasien. Pada bulan Oktober, datanya menunjukkan kemanjuran sekitar 50%, berdasarkan data dari 775 pasien. Obat yang dinamakan molnupiravir ini dikembangkan dengan mitra Ridgeback Biotherapeutics.
Kemanjuran obat Merck yang lebih rendah dapat memiliki implikasi besar dalam hal apakah negara-negara akan terus membeli pil tersebut. Data sementara dari 1.200 peserta dalam uji coba Pfizer Inc untuk pil eksperimentalnya, Paxlovid, menunjukkan pengurangan 89% dalam hopsitalisasi dan kematian.
Saham Merck turun 3,5% menjadi $79,39 pada perdagangan pagi.
Merck merilis data sebelum Badan Pengawas Obat dan Makanan AS (FDA) menerbitkan satu set dokumen pada hari Jumat yang dimaksudkan untuk memberi pengarahan kepada panel ahli luar yang akan bertemu pada hari Selasa untuk membahas apakah akan merekomendasikan otorisasi pil tersebut.
Staf badan tersebut tidak membuat rekomendasi mereka sendiri apakah pil tersebut harus disahkan.
Staf FDA meminta panel untuk mendiskusikan apakah manfaat obat lebih besar daripada risikonya dan apakah pengguna obat tersebut harus dibatasi.
Mereka juga meminta komite untuk mempertimbangkan kekhawatiran apakah obat itu dapat mendorong virus untuk bermutasi, dan bagaimana kekhawatiran itu dapat dikurangi.
Pil seperti molnupiravir dan Paxlovid dapat menjadi senjata baru yang menjanjikan dalam perang melawan pandemi, karena dapat digunakan sebagai perawatan awal di rumah untuk membantu mencegah rawat inap dan kematian akibat COVID-19. Pil tersebut juga bisa menjadi alat penting di negara dan wilayah dengan akses terbatas ke vaksin atau tingkat inokulasi rendah.
PENGOBATAN LEBIH MUDAH
Pil Merck dan Pfizer lebih murah untuk diproduksi dan lebih mudah diberikan daripada pilihan pengobatan yang ada seperti terapi antibodi dari Regeneron dan Eli Lilly, yang sebagian besar diberikan sebagai infus intravena.
Kedua obat eksperimental memiliki mekanisme aksi yang berbeda. Merck dirancang untuk memasukkan kesalahan ke dalam kode genetik virus. Sedangkan obat Pfizer, bagian dari kelas yang dikenal sebagai protease inhibitor, dirancang untuk memblokir enzim yang dibutuhkan virus corona untuk berkembang biak.
Merck mengajukan otorisasi untuk pil molnupiravir mereka di AS pada 11 Oktober 2021, dengan memberikan data sementara, dan kemudian menyerahkan data yang diperbarui ke FDA minggu ini.
Kelompok molnupiravir dari penelitian ini memiliki tingkat rawat inap dan kematian 6,8%, menurut data yang diperbarui. Kelompok plasebo memiliki rawat inap dan tingkat kematian 9,7%.
Satu pasien dalam kelompok molnupiravir meninggal, dibandingkan sembilan pada kelompok plasebo.
Inggris Raya sudah menyetujui penggunaan molnupiravir, disahkan sebagai Lagevrio, awal bulan ini.
Merck mengharapkan untuk memproduksi 10 juta kursus perawatan pada akhir tahun ini, dengan setidaknya 20 juta akan diproduksi pada tahun 2022. Merck memiliki kontrak dengan pemerintah AS untuk memasok sebanyak 5 juta paket dengan harga $700 per paket. Beberapa negara lain telah mengamankan jutaan program pil tersebut.
Merck mengatakan data menunjukkan molnupiravir tidak mampu mendorong perubahan genetik pada sel manusia, tetapi pria yang terdaftar dalam uji cobanya harus berpantang dari hubungan heteroseksual atau setuju untuk menggunakan kontrasepsi. Wanita usia subur juga harus menggunakan alat kontrasepsi.
Namun, FDA mengatakan dalam dokumen pengarahannya bahwa ada kekhawatiran keamanan tentang potensi cacat lahir dari obat tersebut dan meminta panel untuk mendiskusikan apakah obat tersebut harus tersedia untuk wanita hamil.


